Os fungos são mais conhecidos por devolverem à Terra matéria orgânica morta, mas cientistas de materiais estão a investigar se, um dia, poderão também ajudar o nosso corpo a reparar-se, sob a forma de hidrogéis especiais.
Hidrogéis para a biomedicina: camadas como pele, cartilagem e músculo
Para ter utilidade em contextos biomédicos, um hidrogel precisa de uma estrutura com várias camadas, semelhante à da nossa pele, cartilagem e músculos. Enquanto alguns engenheiros desenvolvem versões sintéticas que imitam a biologia, investigadores da Universidade do Utah identificaram um hidrogel que, literalmente, tem vida própria.
Marquandomyces marquandii: o fungo que pode tornar-se um hidrogel biointegrado
Marquandomyces marquandii é uma espécie comum de bolor do solo e um candidato promissor para esta função. Este fungo passou por uma espécie de crise de identidade: foi classificado de forma errada como Paecilomyces marquandii até ser transferido para o seu próprio género em 2020. Em breve, poderá acrescentar “hidrogel biointegrado” ao seu currículo.
Os hidrogéis biointegrados são obtidos a partir de organismos que, já se sabe, formam estruturas em rede - cruzadas e intrincadas - potencialmente capazes de substituir os nossos próprios tecidos moles.
“Hidrogéis são considerados uma alternativa promissora para aplicações em regeneração e engenharia de tecidos, suportes para cultura celular, biorreatores celulares e dispositivos vestíveis, graças à sua capacidade de imitarem de perto as propriedades viscoelásticas dos tecidos moles”, escreve o autor principal Atul Agrawal, engenheiro na Universidade do Utah, juntamente com os seus colaboradores.
Porque é que o micélio interessa tanto como biomaterial
Apesar de estarmos mais familiarizados com os cogumelos e com a penugem do bolor, essas estruturas são, na realidade, as partes reprodutivas do organismo. Os fungos são constituídos sobretudo por uma rede de filamentos chamada micélio, geralmente escondida nas profundezas do solo, da madeira ou daquele abacate esquecido no fundo da fruteira. É precisamente esta rede fibrosa e estratificada que tem tornado os fungos um biomaterial tão apelativo para explorar.
“À medida que avançam no crescimento, vão depositando estas paredes transversais que, depois, compartimentam um filamento muito comprido em muitas, muitas células individuais”, explica a micóloga Bryn Dentinger, do Museu de História Natural do Utah. “Eles vão crescer para sempre desde que haja nutrição suficiente por perto… há muito que poderíamos aproveitar desses comportamentos que ainda não foi plenamente explorado.”
Um hidrogel fúngico que não resseca depressa e retém 83% de água
Outros fungos já foram testados pelo seu potencial como hidrogéis biomédicos, mas muitas vezes revelaram-se demasiado quebradiços ou secavam demasiado rapidamente. Com M. marquandii, não foi isso que aconteceu: quando cultivado através de um método de fermentação líquida estacionária, formou um hidrogel capaz de reter até 83 por cento de água.
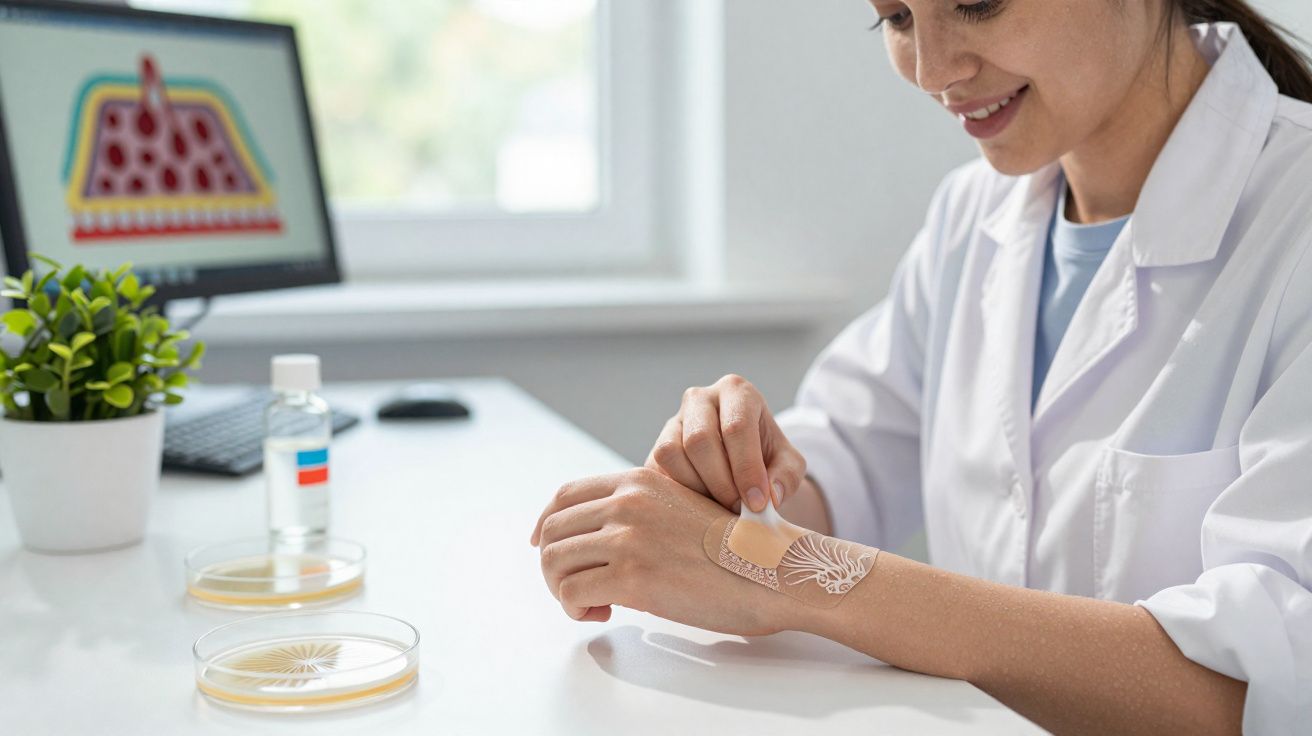
“O que está a ver aqui é um hidrogel com múltiplas camadas”, afirma Agrawal, referindo-se a uma das colónias fúngicas que está a cultivar num frasco de vidro, cheio de um meio de cultura líquido amarelado.
“É visível a olho nu, e estas várias camadas têm porosidades diferentes. Assim, a camada superior tem cerca de 40 por cento de porosidade, e depois há bandas alternadas de 90 por cento de porosidade e 70 por cento de porosidade.”
Os investigadores suspeitam que estas camadas distintas surjam devido a alterações na velocidade e na estratégia de crescimento. Por exemplo, no ponto em que o fungo atingiu a superfície do meio de cultura, a porosidade foi a mais baixa - possivelmente porque a prioridade passou a ser o crescimento lateral. Isto significa que os cientistas poderão ajustar condições de cultivo, como o fornecimento de oxigénio e a temperatura, para optimizar a microestrutura do hidrogel consoante o uso pretendido.
Quitina no micélio: uma “esponja” biocompatível
“Este, em particular, conseguiu desenvolver estas camadas de micélio grandes e robustas, que é exactamente o que nos interessa”, diz Steven Naleway, engenheiro de materiais da Universidade do Utah. “O micélio é feito sobretudo de quitina, que é semelhante ao que existe nas conchas marinhas e nos exoesqueletos dos insectos. É biocompatível, mas também é este tecido extremamente esponjoso.”
“Em teoria, poderia usá-lo como modelo para aplicações biomédicas ou poderia tentar mineralizá-lo e criar uma estrutura de suporte para osso”, acrescenta Naleway.
Segurança e compatibilidade: ainda há muito por testar
Ainda falta muito tempo até um médico poder propor “pele de cogumelo” para tratar queimaduras, ou uma prótese da anca cultivada por fungos. M. marquandii não é conhecido por ser prejudicial para humanos, mas estudos em animais sugerem que a quitina presente no bolor pode desencadear reacções alérgicas raras.
Por outro lado, M. marquandii pode ajudar algumas plantas a crescer. Por isso, serão necessários muitos mais ensaios para perceber quão bem este fungo do solo se dá com tecido vivo - não podemos arriscar um cenário como O Último de Nós.
“Até onde sabemos, este é o primeiro relato de uma espécie de micélio a atingir propriedades tão semelhantes às de um hidrogel sob condições de crescimento submerso, posicionando M. marquandii como um material novo e promissor para aplicações biomédicas”, escreve a equipa.
Esta investigação foi publicada na Revista da Sociedade de Minerais, Metais e Materiais.





Comentários
Ainda não há comentários. Seja o primeiro!
Deixar um comentário